Transcription
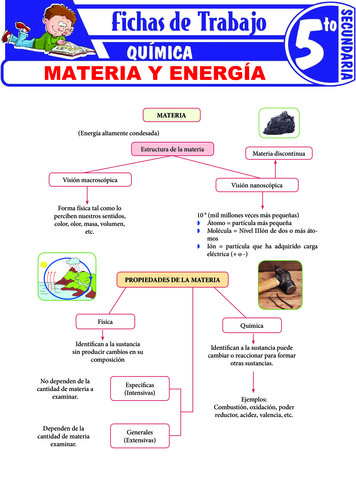
MATERIA Y ENERGÍAMATERIA(Energía altamente condesada)Estructura de la materiaMateria discontinuaVisión macroscópicaVisión nanoscópicaForma física tal como loperciben nuestros sentidos,color, olor, masa, volumen,etc.10-9 (mil millones veces más pequeñas)ZZ Átomo partícula más pequeñaZZ Molécula Nivel IIIón de dos o más átomosZZ Ión partícula que ha adquirido cargaeléctrica ( o -)PROPIEDADES DE LA MATERIAFísicaQuímicaIdentifican a la sustanciasin producir cambios en sucomposiciónNo dependen de lacantidad de materia aexaminar.Especificas(Intensivas)Dependen de lacantidad de materiaexaminar.Generales(Extensivas)Identifican a la sustancia puedecambiar o reaccionar para formarotras sustancias.Ejemplos:Combustión, oxidación, poderreductor, acidez, valencia, etc.
Ejemplos:Propiedades intensivas: Dureza, tenacidad,maleabilidad, ductibilidad, elasticidad, tensión,superficial, viscosidad, punto de ebullición, puntode fusión, conductividad térmica y eléctrica, brillo,densidad calor específico, etc.Propiedad extensiva: Masa, volumen, peso,inercia, extensión, capacidad, calorífica, porosidad,absorbencia, etc.A continuación colocarás entre paréntesis (F) si lapropiedad en físico (Q) si es química:ZZZZZZZZZZZZZZZZZZZZDensidad del gas metano.Punto de ignición del alcoholCombustión de la gasolinaViscosidad del aceiteTensión superficial del mercurioDureza del diamantePresión de vapor del aguaEnergía de ionización del cobreValencia del cloroSolubilidad de la sal en agua(((((((((())))))))))Cóáóbó
Alotropos de carbonoOjo: el grafexona puede ser considerado el sextoalotropo del carbonoVisión nanoscópica de la materiaMezcla HomogéneaMezcla HeterogéneaA continuación colocaras entre paréntesis, si es elemento (E) si es compuesto (C) es mezcla homogénea (mHo)y si es mezcla heterogénea (mHe)ZZZZZZZZZZZZZZZZZZZZZZZZÓxido de calcio(Bronce (Leche de magnesia(Tungsteno (Acero (Ácido clorhídrico (Pólvora (Diamante (Molibdeno (Calcita (Latón (Jugo surtido ())))))))))))ZZZZZZZZZZZZZZZZZZZZZZZZOro (Naftalina (Vinagre (Cloruro de sodio(Ensalada de frutas(Acido muriático (Agua potable (Pirita (Sulfato de sodio(Ozono (Agua oxigenada (Petróleo crudo ())))))))))))
ESTADOS DE AGREGACIÓN DE LA MATERIAMolecularSÓLIDOLÍQUIDOGASEOSOFA FRDesplazamiento porpresiónDefinidoDefinidoBajaFR FADesplazamiento caóticoen todas las direcciónVariableVariableBajísimaFuerzas molecularesF.A.atracciónF.R. repulsiónMovimiento de las partículasFA taPlasmáticoEstado iónico (cargas eléctricas), se encuentra a altas temperaturas y en el universo. Ejemplo: Sol, estrellas, etc.Cambio de estado de agregación de la materiaA continuación completar el siguiente cuadro sobre cambios de estados de la materia:CAMBIO DE AFormación del hielo seco CO2(s)Poner a hervir aguaFormación de las lluviasPreparar adoquines (helados)En los encendedores se tiene gas butano(C4H10*) licuadoDerretir hielo, fundir metalesOlor emanado por la naftalina()NOMBRE DEL CAMBIO DEESTADO
TRANSFORMACIONES DE LA MATERIA (FENÓMENOS)FÍSICASQUÍMICASNo se forman nuevasSe forman nuevas sustanciassustanciasNUCLEARESSe forman nuevas sustanciasNo ocurre cambiosExisten cambios por la ruptura de los Por fisión y fusión nuclear. Hayenlaces entre átomos y formación de desintegración y formación de nuevosnuevos enlaceselementos.Energía bajaEnergía altaEnergía extremadamente altaOJOLos líquidos que cambian de estado rápidamente como la vaporización y en forma espontanea como laacetona, gasolina, bencina, etc, se les denomina volatilización.A continuación coloca entre paréntesis (F) si es una transformación física (Q) si es química (N) si es nuclear.ZZ Combustión de la gasolina()ZZ Fotosíntesis ()ZZ Catabolismo de las enzimas()ZZ Fisión del uranio()ZZ Disolver sal en agua()ZZ Fusión del hidrógeno()ZZ Pulsera de oro de 18 kilates()ZZ Fusión de la parafina de una vela()ZZ Fermentación de la jora()ZZ Liberación de energía del sol()RELACIÓN: MATERIA – ENERGÍAEcuación de Albert EinsteinLey de Conservación materia – energía“La materia y la energía se pueden interconvertir mutuamente pero la suma total de ambas permanece constanteen el Nivel IIIverso”E m . c2Donde:2Joule kg f9 # 1016 m2 ps220 cmErgios g f9 # 10ps2E energía liberada o absorbidaM masa de los productos de la reacciónC velocidad de la luz 3 108 m/s; 3 1010 cm/sSabías quePremio Nobel: 2012Robert Lefkowitz y Brian KobilkaPor su estudios sobre los receptores acoplados a laproteína G.
Trabajando en ClaseNivel INivel II1. La proposición correcta respecto a la materia es:a) Esta formado por átomos y moléculas, pero nopor iones.b) Las mezclas homogéneas están constituidos dedos o más fasesc) Las sustancias no tienen composición definidad) las mezclas heterogéneas están constituidas deuna sola fase.e) Las moléculas son partículas formados por launión química de dos o más átomosResolución:Toda molécula al ser un tipo de sustancia puraestá formada por dos o más átomos.5. El proceso que representa una transformaciónfísica es:a) La transformación del hierro en óxido férricob) La conversión del hidrogeno en helioc) La sublimación del yodod) La combustión de la glucosa en nuestroorganismo.e) La neutralización de la acidez del estomagocon leche magnesia2. La proposición correcta respecto a la materia es:a) Continua, debido a que presenta espaciosvacíos.b) Una solución es una clase de materia homogénea porque el unirse presentan dos o más fasesdiferentes.c) Las sustancias puras más simples son los elementos químicos.d) Las mezclas pueden ser elementos ocompuestos.e) Toda la materia tiene masa pero no volumen3. La relación correcta esa) Amalgama: Mezcla heterogéneab) Bronce : Elementoc) Cobre : Elementod) Aire: sustanciae) grafito: compuesto4Las siguientes son representaciones de la materiaa escala atómica. La asociación correcta es:6. El proceso que representa una transformaciónquímica es:a) El cambio del agua de líquido a vaporb) La desintegración radiactiva del uranioc) La dilatación de una barra de cobre poraumento de temperaturad) La respiración aeróbica que convierte eloxigeno (O2) en dióxido de carbono (CO2)e) La fusión de la parafina de una vela7. Es una característica de las transformacionesfísicas:a) se forman nuevas sustanciasb) se presentan cambios en la estructura internade la materia.c) el cambio implica formación de nuevos elementos.d) la energía involucrada es altae) solo cambia la apariencia externa de la materia.8. Es una propiedad extensiva de la materiaa) Tensión superficialb) Punto de fusiónc) Densidadd) Volumene) Maleabilidad9.a) Compuesto - Mezcla homogénea – mezcla heterogéneab) Compuesto – mezcla homogénea – alótroposc) Elemento – mezcla homogénea – mezcla heterogénead) Elemento – compuesto - mezcla heterogéneae) Mezcla homogénea - compuesto- alótroposEs una propiedad intensiva de la materia:a) Pesob) Volumenc) Absorbanciad) Capacidade) Punto de ebullición
TareaNivel I1. ¿Qué concepto define mejor lo que es una sustanciaquímica (o especie química)a) Es una materia formada por una clase de átomos.b) Es materia homogénea con composicióndefinida (atómica o molecular); por lo tanto conpropiedades especificas definidas y constantes,c) Es la materia homogénea formado concomposición variabled) Toda materia puede ser homogénea o heterogéneae) La materia homogénea está formada solo porátomos de una misma especie.2. Señala (V) si es verdadero o (F)Si es falso a las siguientes proposiciones:I. Una sustancia química tiene composición definida.II. Todo compuesto es una sustancia puraIII. El agua potable es un compuestoIV. El O2, Cl2, F2, Br2 y Pu son elementos simplesa) VVVVb) FFFFc) VVFVd) VFVFe) FFVFd) Diamantee) HelioNivel II4. No es considerada materia:a) Aguab) Gelatinac) Sonidoa) solo Ib) II y IIIc) I y IId) I y IIe) Todas7. De la relación:( ) Salmuera( ) Hielo seco( ) Agua( ) Alcohol yodada(((())))Cal vivaDiamanteGasolinaplataIndica “M” Si es Mezcla “E”, si es Elemento y“C” a los Compuestos. ¿Cuántas son las mezclas,elementos y compuestos, respectivamente?a) 3, 1 y 4b) 2, 2 y 4c) 3, 2 y 3d) 2, 1 y 5e) 4, 2 y 2Nivel III3. ¿Cuál de las siguientes clases de materia representauna mezcla?a) Ozonob) Aceroc) Grafito6. ¿Cuál o cuáles son cambios químicos?I. Cuando el agua se congela.II. Agriado de la lecheIII. Combustión de la gasolinad) Airee) Caballo5. ¿Cuál no es un fenómeno químico?a) Disolución del azúcar en el aguab) Fermentación de la glucosac) Oxidación del hierrod) La respiracióne) Crecimiento de una planta8. Si la masa de 40 gramos de una sustanciaradioactiva, se descompone la décima parte;determina la cantidad de energía en ergiosliberado.a) 36 1020 ergb) 36 1021ergc) 36 1028 ergd) 45 1020 erge) 36 1024 erg9. En una explosión nuclear se usaron “X” gramosde un explosivo generándose 36 1021erg deenergía, si los residuos sólidos tienen una masade 50 gramos. Hallar “X”a) 80 gb) 10 gc) 90 gd) 40 ge) 120 g
b) se presentan cambios en la estructura interna de la materia. c) el cambio implica formación de nuevos ele-mentos. d) la energía involucrada es alta e) solo cambia la apariencia externa de la materia. 8. Es una propiedad extensiva de la materia a) Tensión superficial b) Punto de fusión c) Densidad d) Volumen e) Maleabilidad 9.










